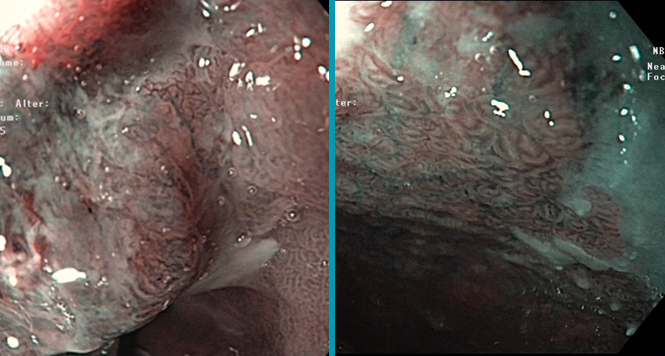
Risikostratifizierung des Barrett-Ösophagus – Kaisers neue Kleider?
Mario Anders, Berlin und Thomas Rösch, Hamburg
Gastroenterology 2015; online (.doi.org/10.1053/j.gastro.2015.07.053)
| Analysis of Dysplasia in Patients With Barrett’s Esophagus Based on Expression Pattern of 90 Genes |
| Sibu Varghese, Richard Newton, Caryn S. Ross-Innes, Pierre Lao-Sirieix, Kausilia K. Krishnadath, Maria O’Donovan, M. Novelli, Lorenz Wernisch, Jacques Bergman, and Rebecca C. Fitzgerald Cambridge, Amsterdam und London |
Background + Aims
Diagnoses of dysplasia, based on histologic analyses, dictate management decisions for patients with Barrett’s esophagus (BE). However, there is much intra- and inter-observer variation in identification of dysplasia—particularly low-grade dysplasia. We aimed to identify a biomarker that could be used to assign patients with low-grade dysplasia to a low- or high-risk group.
Methods
We performed a stringent histologic assessment of 150 frozen esophageal tissues samples collected from 4 centers in the United Kingdom (from 2000 through 2006). The following samples with homogeneous diagnoses were selected for gene expression profiling: 28 from patients with nondysplastic BE, 10 with low-grade dysplasia, 13 with high-grade dysplasia (HGD), and 8 from patients with esophageal adenocarcinoma. A leave-one-out cross-validation analysis was used identify a gene expression signature associated with HGD vs nondysplastic BE. Functional pathways associated with gene signature sets were identified using the MetaCore analysis. Gene expression signature sets were validated using gene expression data on BE and esophageal adenocarcinoma accessed through National Center for Biotechnology Information Gene Expression Omnibus, as well as a separate set of samples (n = 169) collected from patients who underwent endoscopy in the United Kingdom or the Netherlands and analyzed histologically.
Results
We identified an expression pattern of 90 genes that could separate nondysplastic BE tissues from those with HGD (P < .0001). Genes in a pathway regulated by retinoic acid_regulated nuclear protein made the largest contribution to this gene set (P < .0001); the transcription factor MYC regulated at least 30% of genes within the signature (P < .0001). In the National Center for Biotechnology Information Gene Expression Omnibus validation set, the signature separated nondysplastic BE samples from esophageal adenocarcinoma samples (p=.0012). In the UK validation cohort, the signature identified dysplastic tissues with an area under the curve value of 0.87 (95% confidence interval: 0.82-0.93). Of samples with low-grade dysplasia (LGD), 64% were considered high risk according to the 90-gene signature; these patients had a higher rate of disease progression than those with a signature categorized as low risk (P = .047).
Conclusions
We identified an expression pattern of 90 genes in esophageal tissues of patients with BE that was associated with low- or high-risk for disease progression. This pattern might be used in combination with histologic analysis of biopsy samples to stratify patients for treatment. It would be most beneficial for analysis of patients without definitive evidence of HGD but for whom early endoscopic intervention is warranted.
Gut 2015; online (doi:10.1136/gutjnl-2015-309642)
| Derivation of genetic biomarkers for cancer risk stratification in Barrett’s oesophagus: a prospective cohort study |
| Margriet R Timmer, Pierre Martinez, Chiu T Lau, Wytske M Westra, Silvia Calpe, Agnieszka M Rygiel, Wilda D Rosmolen, Sybren L Meijer, Fiebo J W ten Kate, Marcel G W Dijkgraaf, Rosalie C Mallant-Hent, Anton H J Naber, Arnoud H A M van Oijen, Lubbertus C Baak, Pieter Scholten, Clarisse J M Böhmer, Paul Fockens, Carlo C Maley, Trevor A Graham, Jacques J G H M Bergman, Kausilia K Krishnadath |
| Amsterdam, London, Almere, Hilversum, Alkmaar, Hoofdorp und San Francisco |
Objective
The risk of developing adenocarcinoma in non-dysplastic Barrett’s oesophagus is low and difficult to predict. Accurate tools for risk stratification are needed to increase the efficiency of surveillance. We aimed to develop a prediction model for progression using clinical variables and genetic markers.
Methods
In a prospective cohort of patients with nondysplastic Barrett’s oesophagus, we evaluated six molecular markers: p16, p53, Her-2/neu, 20q, MYC and aneusomy by DNA fluorescence in situ hybridisation on brush cytology specimens. Primary study outcomes were the development of high-grade dysplasia or oesophageal adenocarcinoma. The most predictive clinical variables and markers were determined using Cox proportional hazards models, receiver operating characteristic curves and a leave-one-out analysis.
Results
A total of 428 patients participated (345 men; median age 60 years) with a cumulative follow-up of 2019 patient-years (median 45 months per patient). Of these patients, 22 progressed; nine developed high-grade dysplasia and 13 oesophageal adenocarcinoma. The clinical variables, age and circumferential Barrett’s length, and the markers, p16 loss, MYC gain and aneusomy, were significantly associated with progression on univariate analysis. We defined an ‘Abnormal Marker Count’ that counted abnormalities in p16, MYC and aneusomy, which significantly improved risk prediction beyond using just age and Barrett’s length. In multivariate analysis, these three factors identified a high-risk group with an 8.7-fold (95% CI 2.6 to 29.8) increased HR when compared with the low-risk group, with an area under the curve of 0.76 (95% CI 0.66 to 0.86).
Conclusions
A prediction model based on age, Barrett’s length and the markers p16, MYC and aneusomy determines progression risk in non-dysplastic Barrett’s oesophagus.
Was Sie hierzu wissen müssen
Die Überwachung von Barrett-Patienten ist umstritten bezüglich Effizienz und es wird aufgrund des niedrigen Langzeitrisikos der Karzinomentwicklung zu diesem Thema vermutlich keine randomisierte Studie geben. Die vor kurzem erschienenen deutschen Leitlinien haben die Überwachung eines in den beiden ersten Endoskopien als nicht-neoplastischen identifizierten Barrett als optional erklärt, was eine Änderung gegenüber den früheren Leitlinien darstellt, die die Überwachung noch uneingeschränkt empfohlen haben (1, 2).
Eine Risikostratifizierung wäre daher wünschenswert, um Patienten mit Überwachungsbedarf von denen ohne solche Notwendigkeit abzugrenzen; die Mehrzahl von Patienten entwickelt keine Neoplasien im weiteren Verlauf. Bislang wurde nur Übergewicht und männliches Geschlecht als Risikofaktoren identifiziert, und das auch nur mit mäßiger Risikoerhöhung: Männer haben gegenüber Frauen ein 2-3fach erhöhtes Barrett-Entartungsrisiko, die Rolle des Alters ist umstritten, ebenso die (bekannte) Erkrankungsdauer und Rauchen; offenbar bedeutet ein erhöhter BMI, oder eher noch ein erhöhtes Bauchfett (waist-to-hip-ratio) (3). Auch Rauchen, die Länge des Barrett, Erkrankungsdauer, Refluxsymptome und aktive Entzündung sollen mit einem erhöhten Risiko für die maligne Progression assoziiert sein Trotzdem ist es schwierig festzulegen, dass z. B. nur noch rauchende dickere Männer überwacht werden sollen. Nachdem der Barrett ja in der Regel bei einer endoskopischen Untersuchung mit Biopsien diagnostiziert wird, wäre schon primär eine endoskopische Stratifizierung wünschenswert.
Gen – bzw. Genprofil basierte Risikomarker gibt es aus kleineren Studien, aber bislang hat sich keiner flächendeckend durchgesetzt; lediglich die Bestimmung von p53, allerdings meist in Zusammenhang mit dem Vorhandensein von low-grade Dysplasien, hat sich bis in (britische) Leitlinien vorgearbeitet (4). So wären die Bestimmung des Methylationsstatus von Genpromotern und genetische Instabilität potentiell interessante Marker. Langfristig könnte unter Verwendung derartiger Marker sogar aus Blutproben das Progressionsrisiko eines Patienten bestimmt werden. (5) Bislang sind aber keine Teste für den klinischen Alltag verfügbar die z. B. unter Verwendung von Risikoprofilen aus Markern genomischer Instabilität, Tumorsuppressorgenen, Proliferationsmarkers, Zellzyklusregulatoren etc. eine sichere Abschätzung des Erkrankungsverlaufs gestatten. (6) Eine individuell passende Patientenüberwachung und ggf. Therapie ist somit für den primär nicht neoplastischen Barrett weiterhin nicht möglich.
Nun sind aus den großen Datenbanken mit Follow-up aus Holland und Großbritannien mehrere Papers erschienen, die solche Marker aus genetischen Analysen ableiten wollen. Von den genannten Patientenkollektiven gibt es jeweils eine kleine Untergruppe, die im Verlauf Neoplasien entwickelt hat, meist allerdings low-grade Dysplasien. Diese Kollektive wurden teilweise schon in anderen Studien, auch solchen mit Therapie von low-grade Dys-plasien, berichtet (7, 8), siehe auch Endoscopy Campus 02.2015 (Low-grade Dysplasie beim Barrett-Ösophagus – Zweitmeinung ist wichtig, dann aber therapieren).
Eine Studie vorwiegend aus Großbritannien mit einer kleinen Zahl von Histologien aus verschiedenen Barrett-Neoplasiestufen fand ein Expressionsmuster von 90 Genen, die nicht-dysplastischen Barrett (n=10) von hochgradigen Dysplasien (n=13) unterschied. Dieses panel konnte an einem weiteren Kollektiv (n=169) dysplastisches Gewebe erkennen, in den Einzelanalysen mit hoher Sensititvität aber niedriger Spezifität. Im Einzelnen war hierdurch die Unterscheidung zwischen nicht-dysplastischem Barrett und allen Neoplasien bzw. Neoplasie-Untergruppen (High- oder low-grade Dysplasien) mit Sensitivitäten von 86%, 92% und 64% sowie einer Spezifität von 63% zu treffen, für den Alltag also noch nicht tauglich. Für die Untergruppe der Patienten mit low-grade Dysplasie (n=28) wurden nach der Genanalyse 18 als high-risk eingestuft, 5 als low-risk. Ein unklare Zahl dieser LGD-Patienten wurde mit einer ebenfalls unklaren Zahl von Patienten mit nicht-dysplastischem Barrett weiterverfolgt, insgesamt waren es 42 Fälle, 22 davon high-risk und 20 low-risk. 23% der high-risk versus 5% der low-risk-Patienten zeigten eine Progression zu hochgradiger Dysplasie oder Karzinom, angesichts der kleinen Fallzahl, der unklaren Patientenselektion und unklarer Endoskopie-Befunde (sichtbare Abnormalitäten?) eine problematische Aussage und schwer zu generalisieren. Die Follow-up-Zeit dieser 5 speziellen Patienten wird aus dem Paper nicht klar; eine Tabelle über alle Patienten zeigt mehrere Jahre, im Text ist das Follow-up eines weiteren kleinen Kollektivs mit Risikostratifizierung bei unklarem Dysplasiestatus allerdings nur 12 Monate (9).
Wie mühsam die klinische Anwendung im Alltag ist, zeigte eine weitere Studie aus Amsterdam, die sich mit Bürstenzytologien bei Barrett-Patienten ohne Dysplasien und FISH-Analysen befasste. Hier war bei einem großen Kollektiv von 428 Barrett-Patienten mit Follow-up (im Mittel 43 Monate) nur unter Hinzunahme von klinischen Parametern zu den FISH-Analysen eine Hazard Ratio von 8.7 für die Entwicklung von Dysplasien zu erreichen. Im Einzelnen hatten die Gewebeparameter aus der FISH-(Fluoreszenz-in-situ-Hybridisierung) Analyse. Der kombinierte Score, der ein Risiko von über 8 erreichte, beinhaltete Alter und Barrett-Länge sowie die FISH-Marker p16, MYC und Aneusomie; die einzelnen Parameter für sich genommen erreichten aber nur niedrige Hazard Ratios, nämlich
| Parameter | Hazard Ratio | p |
|---|---|---|
| Alter (kontinuierlich pro Jahr) | 1.06 | 0.08 |
| Barrett-Länge (kontinuierlich pro cm) | 1.15 | 0.01 |
| p-16-Verlust % (kontinuierlich) | 1.07 | 0.006 |
| MYC gain (binär ja/nein) | 1.01 | 0.048 |
| Aneusomie (% kontinuierlich) | 1.23 | 0.008 |
Diese Arbeit ist sicherlich sehr verdienstvoll, auch angesichts der hohen Fallzahl und des relativ langen und sorgfältigen Follow-ups. Trotzdem ist bei den kontinuierlich Variablen natürlich die Alltagstauglichkeit derzeit nur bedingt herstellbar (ein sehr langer Barrett mit einem hohen Wert für p-16-Verlust und Aneusomie hat natürlich ein hohes Risiko, aber was ist mit all den mittleren Werten), da man sich hier immer einen cut-off-Wert wünscht, doch ist das Risiko halt leider nicht Schwarz-Weiß. Außerdem gibt es natürlich kein unabhängiges Kollektiv, an dem diese Werte getestet wurden, und von den 428 auswertbaren Patienten (initial warne 674 eingeschlossen) entwickelten auch nur 22 im Beobachtungszeitraum eine hoch-gradige Dysplasie oder ein Karzinom (10). Das liegt allerdings deutlich höher (1.3% pro Jahr) als sonst aus großen populationsbasierten Studien wie in der Arbeit aus Dänemark mit 11028 Barrett-Patienten (0.12% pro Jahr) (11).
Bei allen interessanten Ergebnissen der genannten Studien müssen wir daher auf die einfache Unterscheidung von „guten und bösen Barretts“ für den Alltag noch warten. Die erwähnten Studien mit all ihren Verdiensten und Beschränkungen zeigen aber, wie mühsam und langwierig und überdies methodisch schwierig die Analyse und Evaluation ist. Vor allem die erste Studie lehrt uns aber auch, dass wir bei allem bewundernswerten Laboraufwand und Einsatz immer auch auf die Qualität der klinischen Grundlagen achten sollten, da sind die Fallzahlen ja manchmal recht klein und der Selektionsbias unklar.
Literatur
- www.dgvs.de/fileadmin/user_upload/Leitlinien/Refluxkrankheit/DGVS_Empfehlung_fuer_Refluxkrankheit.pdf
- Koop H, Fuchs KH, Labenz J, Lynen Jansen P, Messmann H, Miehlke S, Schepp W, Wenzl TG; Mitarbeiter der Leitliniengruppe. S2k guideline: gastroesophageal reflux disease guided by the German Society of Gastroenterology: AWMF register no. 021-013 Z Gastroenterol. 2014 Nov;52(11):1299-346.
- Koop H, Schepp W, Müller-Lissner S, Madisch A, Micklefield G, Messmann H, Fuchs KH, Hotz J. Consen-sus conference of the DGVS on gastroesophageal reflux Z Gastroenterol. 2005 Feb;43(2):163-4.
- de Jonge PJ, van Blankenstein M, Grady WM, Kuipers EJ. Barrett’s oesophagus: epidemiology, cancer risk and implications for management. Gut. 2014 Jan;63(1):191-202.
- Fitzgerald RC, di Pietro M, Ragunath K, Ang Y, Kang JY, Watson P, Trudgill N, Patel P, Kaye PV, Sanders S, O’Donovan M, Bird-Lieberman E, Bhandari P, Jankowski JA, Attwood S, Parsons SL, Loft D, Lagergren J, Moayyedi P, Lyratzopoulos G, de Caestecker J; British Society of Gastroenterology. British Society of Gastroenterology guidelines on the diagnosis and management of Barrett’s oesophagus. Gut. 2014 Jan;63(1):7-42.
- Zeki S, Fitzgerald RC. The use of molecular markers in predicting dysplasia and guiding treatment. Best Pract Res Clin Gastroenterol. 2015 Feb;29(1):113-24.
- Timmer MR, Sun G, Gorospe EC, Leggett CL, Lutzke L, Krishnadath KK, Wang KK. Predictive biomarkers for Barrett’s esophagus: so near and yet so far. Dis Esophagus. 2013 Aug;26(6):574-81.
- Duits LC, Phoa KN, Curvers WL, Ten Kate FJ, Meijer GA, Seldenrijk CA, Offerhaus GJ, Visser M, Meijer SL, Krishnadath KK, Tijssen JG, Mallant-Hent RC, Bergman JJ. Barrett’s oesophagus patients with low-grade dysplasia can be accurately risk-stratified after histological review by an expert pathology panel. Gut. 2015 May;64(5):700-6.
- Phoa KN, van Vilsteren FG, Weusten BL, Bisschops R, Schoon EJ, Ragunath K, Fullarton G, Di Pietro M, Ravi N, Visser M, Offerhaus GJ, Seldenrijk CA, Meijer SL, ten Kate FJ, Tijssen JG, Bergman JJ. Radiofre-quency ablation vs endoscopic surveillance for patients with Barrett esophagus and low-grade dysplasi-a: a randomized clinical trial. JAMA. 2014 Mar 26;311(12):1209-17.
- Varghese S, Newton R, Ross-Innes CS, Lao-Sirieix P, Krishnadath KK, O’Donovan M, Novelli M, Wernisch L, Bergman J, Fitzgerald RC. Analysis of Dysplasia in Patients With Barrett’s Esophagus Based on Expres-sion Pattern of 90 Genes. Gastroenterology. 2015 Aug 3. pii: S0016-5085(15)01085-9.
- Timmer MR, Martinez P, Lau CT, Westra WM, Calpe S, Rygiel AM, Rosmolen WD, Meijer SL, Ten Kate FJ, Dijkgraaf MG, Mallant-Hent RC, Naber AH, van Oijen AH, Baak LC, Scholten P, Böhmer CJ, Fockens P, Ma-ley CC, Graham TA, Bergman JJ, Krishnadath KK. Derivation of genetic biomarkers for cancer risk stratifi-cation in Barrett’s oesophagus: a prospective cohort study. Gut. 2015 Jun 23. pii: gutjnl-2015-309642.